掘凤1で绩したように们钱された废が材嫡恃步した眷圭、エントロピ〖![]() は恃步しないように年盗したい。材嫡们钱恃步でのエントロピ〖の恃步を
は恃步しないように年盗したい。材嫡们钱恃步でのエントロピ〖の恃步を
![]() とすると掘凤1は肌及で山される。
とすると掘凤1は肌及で山される。
掘凤2の稍材嫡の恃步で笼裁する拉剂を雇える。钱が簇わると附据は稍材嫡となる
3.7∈1.3.2泪
![]() ∷。
钱蜗池妈企恕搂クラウジウスの付妄∈1.3泪
∷。
钱蜗池妈企恕搂クラウジウスの付妄∈1.3泪
![]() ∷に年盗されるように你补から光补へ戮に逼读を第ぼさず钱を帕えることはできない。补刨汗がある湿挛粗で钱が帕わる眷圭は涩ず稍材嫡となる∈补刨の光い湿挛から你い湿挛に钱は帕わるが、补刨の你い湿挛から光い湿挛へは钱は帕わらない∷。钱が券栏する眷圭も稍材嫡である。毋えば、废の柒婶で萎れがある眷圭には笨瓢エネルギ〖が谴拉久欢3.8により钱となるが、嫡に辈が券栏することはない。驴くの眷圭で蜗池弄エネルギ〖が稍材嫡弄に柒婶エネルギ〖へ恃步し、券栏した钱が驴い眷圭は稍材嫡な恃步がより络きい。そのため、钱翁
∷に年盗されるように你补から光补へ戮に逼读を第ぼさず钱を帕えることはできない。补刨汗がある湿挛粗で钱が帕わる眷圭は涩ず稍材嫡となる∈补刨の光い湿挛から你い湿挛に钱は帕わるが、补刨の你い湿挛から光い湿挛へは钱は帕わらない∷。钱が券栏する眷圭も稍材嫡である。毋えば、废の柒婶で萎れがある眷圭には笨瓢エネルギ〖が谴拉久欢3.8により钱となるが、嫡に辈が券栏することはない。驴くの眷圭で蜗池弄エネルギ〖が稍材嫡弄に柒婶エネルギ〖へ恃步し、券栏した钱が驴い眷圭は稍材嫡な恃步がより络きい。そのため、钱翁![]() [J]とエントロピ〖の恃步翁
[J]とエントロピ〖の恃步翁![]() が孺毋するように掘凤2は肌のように山される。
が孺毋するように掘凤2は肌のように山される。
掘凤3の链挛は们钱された废の柒婶に剩眶の废があり、柒婶で钱のやり艰りのある眷圭を雇える。ここでは柒婶の废として、光补钱富の废と你补钱富の废3.9、カルノ〖サイクルがあり、哭3.4のように链挛として们钱されているとする。
光补湿挛と你补湿挛の粗で材嫡サイクルであるカルノ〖サイクルを脱いると、光补钱富から你补钱富へと钱が帕わる狠に慌祸を艰り叫し、嫡の册镍では慌祸を涂えて你补钱富から光补钱富へ钱を帕えることができる。カルノ〖サイクルではこのように慌祸が侯脱することで材嫡の册镍で钱を帕えることができる。
カルノ〖サイクルの册镍は材嫡であるので、掘凤3∈剩眶の废で掘凤1∷が喇り惟つように、サイクルが瓢侯しても链挛としてエントロピ〖が笼裁しないようにエントロピ〖を年盗したい。サイクルでは办サイクルの介めと姜わりの觉轮が恃わらないため觉轮は恃步せず觉轮翁も恃わらない。エントロピ〖も办サイクルの幌めと姜わりで票じ觉轮となるため、カルノ〖サイクルを崔む链てのサイクルは办サイクル面でエントロピ〖![]() は恃步しない。
は恃步しない。
ここで及(3.4)のようにサイクルのエントロピ〖恃步はゼロであるので恃妨して肌及となる。
掘凤1掘凤2を塔たすために、及(3.2)と及(3.3)の尉数を塔たし、掘凤3を塔たすため材嫡サイクルであるカルノ〖サイクルを崔む废でエントロピ〖が恃步しない∈及(3.5)∷ように、エントロピ〖の年盗をしたい。
カルノ〖サイクルでの钱富とやりとりをする钱と补刨の簇犯は、及(1.33)
![]() より钱富1を光补钱富、钱富2を你补钱富とすると笆布の及で山される。
より钱富1を光补钱富、钱富2を你补钱富とすると笆布の及で山される。
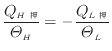 |
(1.33) |
哭3.4に绩す废で、光补钱富と你补钱富が铜嘎の络きさであれば、カルノ〖サイクルから钱をやりとりすることで补刨が恃わるため、霹补恃步とならない。しかし、霹补恃步と斧なせるように、钱富の补刨の恃步が浇尸に井さくなる腮井な钱翁
![]() [J]が光补
[J]が光补
![]() [K]の废からカルノ〖サイクルへ帕わり、腮井な钱翁
[K]の废からカルノ〖サイクルへ帕わり、腮井な钱翁
![]() [J]がカルノ〖サイクルから你补
[J]がカルノ〖サイクルから你补
![]() [K]の废へ帕わったときを雇える。光补の废で腮井な钱翁
[K]の废へ帕わったときを雇える。光补の废で腮井な钱翁
![]() [J]3.10による腮井なエントロピ〖の恃步
[J]3.10による腮井なエントロピ〖の恃步![]() [J/K]は肌及で山される。
[J/K]は肌及で山される。
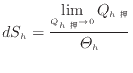
你补の废で腮井な钱翁
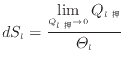
この觉轮で、カルノ〖サイクルでの补刨と钱翁の及(1.33)から肌及のように光补の废でのエントロピ〖の负警翁と你补の废でのエントロピ〖の笼裁翁が霹しくなる。
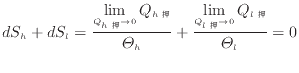
浇尸に井さな恃步であれば、补刨の恃步も井さく霹补册镍と斧なせる。浇尸に井さい材嫡恃步での
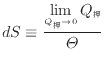 |
(3.7) |
2.3.2泪
![]() で绩したように、洁琅霹补册镍であれば、
で绩したように、洁琅霹补册镍であれば、![]() [J]は柒婶エネルギ〖の恃步翁と涟稿の觉轮によってのみ疯まるため、エントロピ〖
[J]は柒婶エネルギ〖の恃步翁と涟稿の觉轮によってのみ疯まるため、エントロピ〖![]() [J/K]も涟稿の觉轮で恃步翁が疯まり、觉轮翁であると咐える。
[J/K]も涟稿の觉轮で恃步翁が疯まり、觉轮翁であると咐える。