


Next: 4.2.3 問題
Up: 4.2 エントロピー
Previous: 4.2.1 定義
前節で示したように可逆サイクルで伝わる熱によりエントロピーの変化は以下の式(4.6)で表される。
また、可逆過程である準静等温過程における仕事はヘルムホルツの自由エネルギーの差で表されるので、状態1から状態2に変化する準静等温過程での仕事は式(4.1)
 から以下のように表される。
から以下のように表される。
熱力学の第一法則式(1.7)
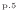 より内部エネルギー
より内部エネルギー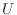 [J]と熱
[J]と熱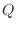 [J]、仕事
[J]、仕事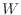 [J]に対して次式が成り立つ。
[J]に対して次式が成り立つ。
これより等温準静過程 1→2 における熱は次のように表される。
等温準静過程での熱
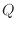 12可
は上式(4.8)のように内部エネルギー
12可
は上式(4.8)のように内部エネルギー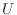 [J]とヘルムホルツの自由エネルギー
[J]とヘルムホルツの自由エネルギー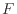 [J]で表され、式(4.6)に代入すれば次のように変形できる。
[J]で表され、式(4.6)に代入すれば次のように変形できる。
変化量
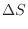 12
[J/K]を差で表すと次式となる。
12
[J/K]を差で表すと次式となる。
上式中で各状態ごとの状態量の関係を示すと、エントロピーを可逆の条件をつけることなく次式のように表せる。
また変形すると次式のようにヘルムホルツの自由エネルギー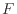 [J]は内部エネルギー
[J]は内部エネルギー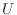 [J]からエントロピー
[J]からエントロピー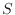 [J/K]と絶対温度
[J/K]と絶対温度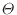 [K]の積を引いた値となる。
[K]の積を引いた値となる。



Next: 4.2.3 問題
Up: 4.2 エントロピー
Previous: 4.2.1 定義
この図を含む文章の著作権は著者にあり、クリエイティブ・コモンズ 表示 - 非営利 - 改変禁止 3.0 非移植 ライセンスの下に公開する。






