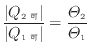 |
(1.32) |
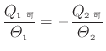 |
(1.33) |
- 1.4.7節
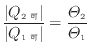 |
(1.32) |
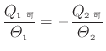 |
(1.33) |
高温の温度
![]() [K]から低温の
[K]から低温の
![]() [K]へ熱が伝わる状況では、伝わる熱を
[K]へ熱が伝わる状況では、伝わる熱を![]() [J]とすると式(1.34)より最大で以下の式で表される仕事
[J]とすると式(1.34)より最大で以下の式で表される仕事![]() [J]を取り出すことができる。
[J]を取り出すことができる。
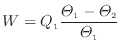
また、発電所のように二つの熱源(火力発電所であれば燃料の燃焼温度と大気や海水の温度)で動作するサイクル(熱機関)の最高の効率は可逆サイクルの効率であり、その効率は熱源の温度により決まる。熱機関においては、どれほど技術が進んでも二つの熱源の温度で決まる効率を超えて熱源から仕事を取り出すことはできない。