


Next: 1.2.6 温度と内部エネルギー
Up: 1.2 熱力学第一法則
Previous: 1.2.4 発熱
系と周囲で物質の出入りがなく系の位置が変わらなければ、系が外部とやりとりする熱の和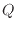 [J]と仕事
[J]と仕事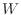 [J]の総和は熱力学第一法則より内部エネルギーの変化量
[J]の総和は熱力学第一法則より内部エネルギーの変化量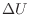 [J]と等しい。熱
[J]と等しい。熱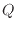 [J]と仕事
[J]と仕事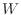 [J]が外部と出入りすることによって内部エネルギーは変化する(
[J]が外部と出入りすることによって内部エネルギーは変化する(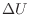 [J])ので、次式で表される(外から伝わり入る方向を正、外へ伝え出る方向を負とする)。
[J])ので、次式で表される(外から伝わり入る方向を正、外へ伝え出る方向を負とする)。
熱力学第一法則、温度、仕事、熱、内部エネルギーの導入方法には何通りかあり、BejanのAdvanced engineering Thermodynamisc[#!2006Bejan!#]の1.8節によくまとめられている。



Next: 1.2.6 温度と内部エネルギー
Up: 1.2 熱力学第一法則
Previous: 1.2.4 発熱
この図を含む文章の著作権は椿耕太郎にあり、クリエイティブ・コモンズ 表示 - 非営利 - 改変禁止 4.0 国際 ライセンスの下に公開する。最新版およびpdf版はhttp://camellia.thyme.jpで公開している。