![\includegraphics[width=50mm]{figures/SimpleCycleVolumeHeatengine.eps}](img56.png)
|
サイクルでは周囲と熱と仕事をやりとりする。それぞれの過程では以下のことが起こっている。
冷却や加熱をされると、圧力が変化し、断熱変化で体積が変化することにより周囲と仕事のやりとりをする。圧力の変化の概略は図1.4のようになる(圧力変化の傾きは例として示したもので、過程によって異なることもある)。図1.5に温度変化の概略を示す(温度変化の傾きは例として示したものである)。断熱圧縮時には温度は上昇し、断熱膨張時には温度は低下する。冷却の後の2→3の過程では、体積が減少することで仕事をされる。加熱の後の4→1の過程では、体積が増加し周囲に仕事をしている。体積増加の際の仕事については付録B.1(p.![[*]](crossref.png) )に詳細を記した。
)に詳細を記した。
仕事![]() [J]は圧力
[J]は圧力![]() [Pa]と微小体積変化
[Pa]と微小体積変化![]() [m
[m![]() ]の積分により
]の積分により
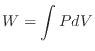
で表される 1.6。 状態2から状態3と状態4から状態1での体積の変化量は同じであるので、仕事の大きさは圧力によって決まる。図1.4から、状態2から状態3の平均圧力より、状態4から状態1の平均圧力が大きいことが分かる。そのため、積分して得られる仕事も大きくなり、以下の式が得られる。状態2から状態3では仕事をされるため正の値、状態4から状態1では仕事をするため負の値となる。そこで、絶対値をとり大きさを比較する。
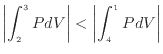
状態2から状態3では周囲から仕事をされ、状態4から状態1では周囲に仕事をしている。このことからこのサイクルでは
![]() の仕事を周囲にしている1.7ことが分かる。また、状態3から状態4で周囲(熱源3-4)から熱を受け取り、状態1から状態2で周囲(熱源1-2)に熱を与えている。図1.5の温度変化の概略に示すように、周囲の温度は状態3から状態4の熱源3-4が状態1から状態2の熱源1-2よりも高い。このことから、このサイクルは高温の熱源3-4から熱を受け取り、低温の熱源1-2へ熱を与えている。
の仕事を周囲にしている1.7ことが分かる。また、状態3から状態4で周囲(熱源3-4)から熱を受け取り、状態1から状態2で周囲(熱源1-2)に熱を与えている。図1.5の温度変化の概略に示すように、周囲の温度は状態3から状態4の熱源3-4が状態1から状態2の熱源1-2よりも高い。このことから、このサイクルは高温の熱源3-4から熱を受け取り、低温の熱源1-2へ熱を与えている。
状態1から再度状態1へ戻るとき、内部エネルギーの値は等しく変化はゼロであるので、エネルギーの保存から以下の式が成り立つ。
![[*]](crossref.png) と上式から、熱の大きさの関係を求める。状態1から状態2では外部に熱を伝えるため負の値となり、状態3から状態4では外部から熱を受け取るため正の値となる。そのため絶対値をとり大きさを比較すると、以下の式が成り立つ。。
と上式から、熱の大きさの関係を求める。状態1から状態2では外部に熱を伝えるため負の値となり、状態3から状態4では外部から熱を受け取るため正の値となる。そのため絶対値をとり大きさを比較すると、以下の式が成り立つ。。
低温熱源へ渡す熱の大きさよりも、高温熱源から受け取る熱の大きさのほうが大きい。以上から、高温熱源から熱を受け取り、一部を仕事に変換し外部へ取り出し、高温熱源から受け取った熱より少ない残りの熱を低温熱源へ渡している。すなわち、熱機関として動作していることがわかる。
実際に世の中で使われている熱機関として火力発電所や原子力発電所がある。発電所のサイクルは閉じた系ではないが、同じように考えられる。発電所の多くでは系の中の物質に水を用いている。発電所と図1.3のサイクルの対応は以下のようになっている。